检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2023年12月15日,js33333金沙线路检测张研课题组、京东方科技集团股份有限公司合作在美国化学会旗舰期刊ACS Nano杂志在线发表了题为High-Performance Plasma Biomarker Panel for Alzheimer’s Disease Screening Using a Femtomolar-Level Label-Free Biosensing System的论文。该研究利用超灵敏石墨烯场效应晶体管(gFET)传感器测定了多中心临床队列人血浆中阿尔茨海默症(AD)生物标志物淀粉样蛋白Aβ40、Aβ42、磷酸化P-tau181、P-tau217和神经丝轻链蛋白(NfL) 含量。同时,该研究采用机器学习算法对这些血浆生物标志物进行组合分析,构建了一个“Composite-Info”生物标志物组合,显著提高了AD进展的分期性能。在接收者操作特征曲线(ROC)上,该组合的曲线下面积(AUC)大于 0.94。此外,与简易精神状态量表(MMSE)/蒙特利尔认知评估(MoCA)和核磁共振成像(MRI)相比,该研究在基于个体的分期评估中表现出优势,为早期筛查AD提供了一个快速的检测诊断系统。
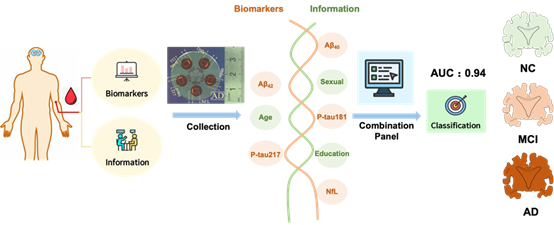
图1:基于多靶标检测的血液筛查阿尔茨海默症方法
AD是老年人痴呆症的主要病因,然而,由于缺乏对阿尔茨海默病理的了解,目前的疗法无法预防或逆转认知能力的下降。轻度认知障碍(MCI)的预后对潜在的老年痴呆症治疗至关重要,因为它既可能发展为痴呆症,也可能保持良性和稳定。此外,在 MCI 阶段,也可以通过脑脊液(CSF)分析或正电子发射断层扫描(PET)成像检测到 AD 的关键生物标志物,如Aβ和P-tau。尽管脑脊液分析和正电子发射断层扫描可提供诊断信息,但由于腰椎穿刺的侵入性以及正电子发射断层扫描的高成本和有限可用性,它们的实施受到了限制。相比之下,检测血液样本中与 AD 相关的生物标志物可为诊断 AD 提供有效而经济的方法。
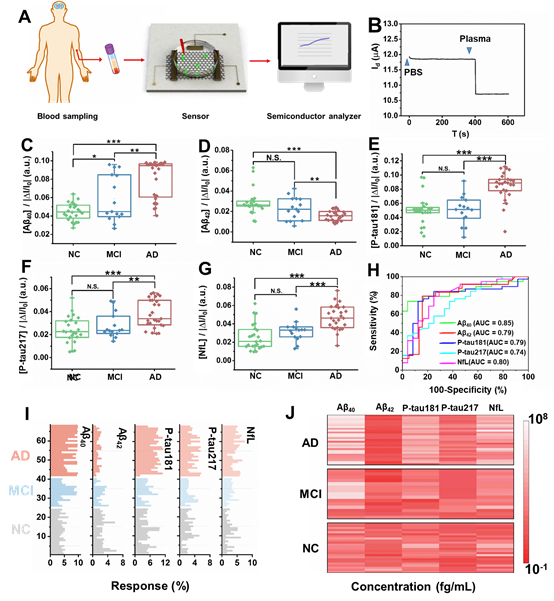
图2:基于自研传感器进行血液样本的多靶标检测结果
迄今为止,用于从健康人群中对AD患者进行分类的相关生物标志物最佳组合仍在开发中,基于血浆的Aβ、tau和神经退行性标志物(如NfL和GFAP等)作为组合进行诊断已经成为当前国际框架共识(ATN体系),目前逻辑回归方法在单标志物判断方法取得了一些进展,有助于开发AD诊断标志物。与此同时,其他分类策略,如随机森林和支持向量机等方法,在样本有限的多变量问题上表现出色。通过这些机器学习方法的组装,可以发现多生物标志物的AD精确诊断方法。此外,血浆中的生物标志物浓度通常比脑脊液中低十倍以上,常规手段很难对血浆进行高性能的AD相关标志物检测。此外,血液成分的复杂性也使准确可靠地检测血液中的生物标志物变得困难。因此,超灵敏检测方法对于有效分析血浆生物标志物至关重要。gFET生物传感器可在数小时内将这些生物标志物的检测限降至飞摩尔水平,从而提供了超灵敏检测血浆中ATN生物标志物的可能。
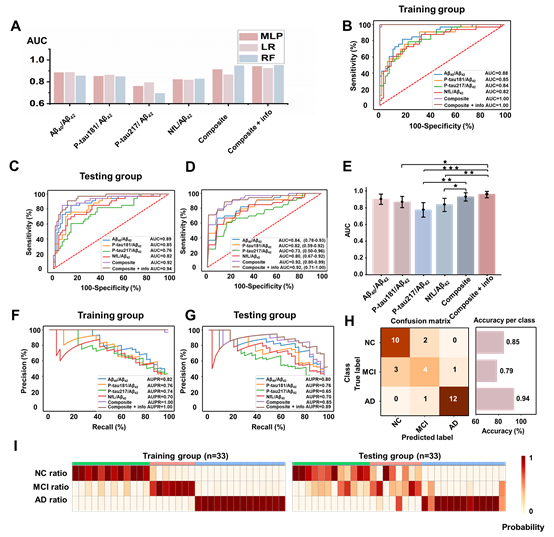
图3:基于诊断模型实现临床样本的三分类区分
针对现存问题,本研究构建了超灵敏gFET装置,并开发了基于多靶标生物标志物的诊断组合。该gFET装置对血浆中的AD生物标记物具有极高的选择性和灵敏度,其LoD达到飞摩尔级。除了飞摩尔灵敏度外,该装置还能选择性地检测血浆中五种与AD相关的生物标记物。通过多种机器学习算法的使用,将多种标志物和临床信息进行有效组合并进行诊断分期,得到表现良好的"Composite-info "生物标志物组合。其可以成功地对NC,MCI和AD患者进行分类,AUC 可达0.94。这项工作提供的一种传感平台和 "Composite-info "生物标志物组合,可用于早期AD诊断,在临床上具有良好的前景。
论文第一作者为js33333金沙线路检测与京东方科技集团联合博士后王世才博士,京东方科技集团邓睿君博士和js33333金沙线路检测博士后陈智雅博士,共同通讯作者为js33333金沙线路检测的张研教授、京东方科技集团的赵子健博士和李延钊博士。该研究获得中国科技部,国家自然科学基金委,js33333金沙线路检测启东产业创新基金,京东方科技集团和朝阳区博士后经费资助等的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.3c09311
研究组介绍
张研:
js33333金沙线路检测教授,膜生物学国家重点实验室PI。
实验室研究领域:
长期从事神经退行性疾病,特别是阿尔茨海默氏症中神经元凋亡及淀粉样沉积的代谢途径的研究工作。利用人类原代神经元为模型研究神经退行性疾病,采用细胞内显微注射系统,将外源性蛋白及表达质粒引入细胞等方法分析胞内淀粉样沉积毒性及其作用通路,为淀粉样沉积导致阿尔茨默症的发病机制提供了新的见解。发现并纯化内源性半胱氨酸蛋白酶抑制因子;提出朊蛋白的细胞保护假说。在此基础上,筛选并研究了一系列可以对抗细胞内淀粉样沉积毒性的物质;发现了包含甘丙肽和吗啡在内的临床应用药物的细胞保护作用并研究了其作用机制和分子通路;发现并阐明神经细胞纳米连接的诱导机制;深入探讨了纳米连接在神经退行性疾病中的作用;发现家族型老年性痴呆的突变可以导致microRNA调节和神经元早期发育的异常;揭示了轴突起始节部位异常和老年性痴呆的病理关系;提出了在遗传性AD突变携带者中,神经元存在着早期的发育缺陷。近10年来在国际著名的神经生物学和细胞生物学期刊Neuron, PNAS, Cell Reports,Prog Neurobiol, Nat Methods, Nat Protocol, J Cell Biol, Neurosci Biobehav Rev, J Neurosci, Cell Death Differ, Cell Death Dis, JACS, J Cell Sci等发表学术论文。张研教授为诸多国际期刊审稿并担任有影响力的专业期刊的编委。