检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
核糖体催化的蛋白质生物合成是细胞中最精密、最关键的生命活动之一。在肽链延伸过程中,柔性的尚未折叠的新生肽链有错误折叠和引发蛋白质聚集的风险,折叠不正常的新生蛋白质可能通过细胞毒性等机制破坏蛋白质稳态和细胞内环境[1]。除此之外,新生肽链的质量控制还和衰老及特定的病理条件密切相关。例如,近期的一项工作以秀丽隐杆线虫和酿酒酵母为模型,研究了衰老和蛋白质合成的关系,发现在衰老细胞中核糖体翻译延伸停滞机率的增加,尤其是编码碱性氨基酸簇(K/R,polybasic stretches)的mRNA区域,诱发了核糖体翻译质量控制体系的超载和新生多肽的聚集,从而损害了细胞的蛋白质稳态继而造成类型各异的细胞功能衰退[2]。无论是真核还是原核细胞,都具有一系列的共翻译调控系统,在肽链延伸的同时对新生肽链进行修饰、加工,帮助其实现膜定位及辅助其折叠。RAC(ribosome-associated complex)和NAC(nascent chain-associated complex)是真核生物的两种共翻译折叠系统。研究表明酿酒酵母RAC对新生肽链中的poly-lysine序列的合成具有调控作用,表明RAC在折叠功能之外,可能直接参与核糖体上蛋白质翻译调控。
RAC是由Hsp40和Hsp70组成的稳定异源二聚体,在真核生物中高度保守,其在酵母中对应蛋白为Zuo1和Ssz1。Zuo1的J-domain(JD)结构域能够特异招募酵母的另一个Hsp70蛋白质因子Ssb1/2进入到处于新生肽链合成过程中的核糖体复合物(RNC,ribosome-nascent chain complex),并特异激活Ssb的ATPase活性。ATP水解之后的Ssb-ADP与新生肽链稳定结合直到其完成正确的折叠。遗传数据表明,Zuo1、Ssz1、Ssb三者对于新生肽链的正确折叠缺一不可。RAC系统的结构和功能机制一直是翻译调控领域的一个重要研究内容,迄今为止,该系统的具体分子机制的诸多细节尚不清楚,例如一个Hsp40如何与两个Hsp70配合、Hsp70 Ssz1的分子功能、Hsp40 Zuo1如何特异招募Hsp70 Ssb,新生肽链如何与三个蛋白质组分发生相互作用等等。
2022年6月14日,js33333金沙线路检测高宁课题组于Nature Communications在线发表了题为Structural remodeling of ribosome associated Hsp40-Hsp70 chaperones during co-translational folding 的研究论文。该研究以酿酒酵母为模型,利用冷冻电镜技术解析了细胞内源的RAC-80S复合物、不同状态的RAC-RNC复合物的十余个高分辨结构,揭示了RAC-Hsp70系统的构象转变,提出了RAC-Ssb的工作机制模型。
首先,结构分析发现,与课题组2014年发表的首个RAC-核糖体低分辨结构[3]一致,Zuo1的N端和C端结构域在空间上分别结合核糖体的大亚基和小亚基。不同的是,在分辨大幅提高的情况下RAC与核糖体的相互作用细节能够被清楚地呈现。RAC结合在核糖体小亚基40S解码中心的rRNA helix 44末端的Zuo1 4HB结构域使helix 44发生了明显的构象变化,揭示了RAC调控核糖体上的功能中心的结构基础(图1 a)。RAC剩余的部分(Zuo1 NTD)结合在核糖体大亚基60S的肽链通道出口(PTE,peptide exit tunnel),直接和新生肽链发生相互作用。
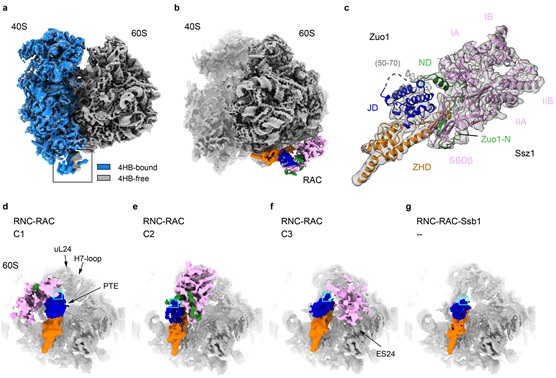
图1不同状态的S. cerevisiae RAC-核糖体复合物冷冻电镜结构
通过针对Zuo1-NTD的局部分类与计算,该研究首次解析了近全长的RAC结构(图1 b-c)。通过解析和对比无新生肽链的RAC-80S复合物、带有新生肽链的RAC-RNC和RAC-RNC(+Ssb1-ATP)复合物的十余个不同状态的结构,该研究发现:(1)在核糖体不进行翻译或新生肽链尚未暴露时,RAC中仅Zuo1与60S相互作用。其中Ssz1远离PTE不与核糖体直接接触,通过对Zuo1 JD形成空间位阻使其不能招募Ssb,处于自抑制状态(图1 d);(2)随着翻译延伸的进行,新生肽链从PTE暴露出来,它首先与Zuo1结合在PTE附近的一小段螺旋结构的疏水表面相互作用,因此Zuo1是RAC-Ssb系统中第一个与新生肽链相互作用的组分;(3)新生肽链的存在还引发了RAC从自抑制状态的构象转变,不同程度地削弱了Ssz1对Zuo1 JD空间阻挡(图1 e-f)。在其中一个较为稳定的构象中,Ssz1进行了大幅度的空间翻转,NBD(nucleotide binding domain)与核糖体相互作用,导致Ssz1罩在PTE正上方,对该空间形成保护之势(图1 e);在 Zuo1-Ssz1-PET包围的空间内有一段对应3-4个氨基酸的电子密度,可能是新生肽链,因此Ssz1可能是RAC-Ssb中第二个与新生肽链发生相互作用的组分;(4)而在RAC-RNC中加入Ssb1-ATP后,解析的所有结构中均没有观察到稳定的Ssz1和Ssb1密度(图1 g);传统的Hsp40和其Hsp70搭档的相互作用是瞬时的,因此推测此时的Ssz1和Ssb1都处于高度动态的构象状态。
基于这些新的结构观察以及已有文献报道,该研究提出了RAC-Ssb系统的工作机制模式图(图2)。在这一过程中,不断延伸的新生肽链通过与系统中的不同蛋白质因子发生相互作用,从而引起级联的构象重组过程,使得RAC-Ssb系统能够高效地捕捉新生肽链上的底物序列,从而及时对这些序列进行保护。综上,该研究揭示了新生肽链引发的RAC构象转变的分子基础,阐述了RAC-Ssb系统中3个组成因子在共翻译折叠过程中分工合作的分子机理(图2),对进一步理解共翻译调控和蛋白质折叠机理具有重要意义。
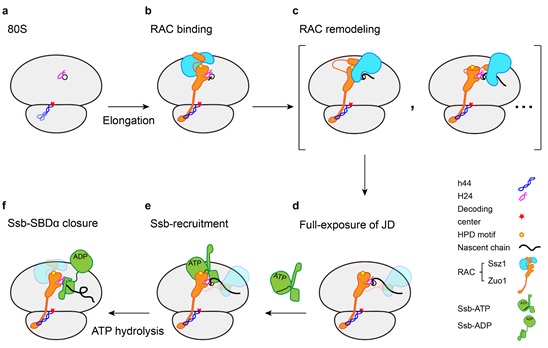
图2 RAC-Ssb共翻译折叠系统的分子机制
高宁教授为该论文的通讯作者,课题组2016级博士生陈燕(已毕业)为本文的第一作者。该研究得到了国家自然科学基金、国家重点研发计划、启东-SLS创新基金、北大-清华生命科学联合中心、膜生物学国家重点实验室的支持。js33333金沙线路检测冷冻电镜平台、电镜实验室、高性能计算平台、js33333金沙线路检测仪器中心及凤凰工程等多个仪器平台对本项目提供了重要的技术支撑。
论文全文:https://www.nature.com/articles/s41467-022-31127-4
1. Rosenzweig, R., et al., The Hsp70 chaperone network. Nat Rev Mol Cell Biol, 2019. 20(11): p. 665-680.
2. Stein, K.C., et al., Ageing exacerbates ribosome pausing to disrupt cotranslational proteostasis. Nature, 2022. 601(7894): p. 637-642.
3. Zhang, Y., et al., Structural basis for interaction of a cotranslational chaperone with the eukaryotic ribosome. Nat Struct Mol Biol, 2014. 21(12): p. 1042-6.